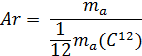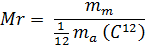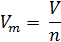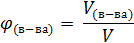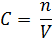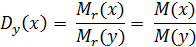|
Разделы
Наш опрос
|
Количественные величины, используемые в химииОтносительная атомная масса (Ar) – отношение массы атома элемента к 1/12 части массы атома изотопа С12.
Относительная молекулярная масса (Mr) – отношение массы молекулы вещества к 1/12 части массы атома изотопа С12.
Относительная молекулярная масса – безразмерная величина, показывающая во сколько раз масса молекулы вещества больше 1 а.е.м. Понятие «относительная молекулярная масса» применяется для веществ молекулярного строения. Для веществ немолекулярного строения пользуются понятием «относительная формульная масса»
Относительная формульная масса вещества – физическая величина, равная отношению массы формульной единицы данного вещества к 1/12 части массы атома изотопа C12.
Молярная масса – отношение массы вещества к его количеству.
[ г/моль; кг/моль]
Молярный объём – отношение объёма вещества к его количеству.
Vm = 22,4 дм3/моль
Массовая доля компонента в веществе – отношение массы компонента, содержащегося в системе к общей массе всей системы.
Молярная доля компонента в веществе – безразмерная величина, равная отношению количества вещества компонента к общему количеству вещества всей системы.
Количество вещества системы – размерная физическая величина, характеризуемая численностью, содержащаяся в системе структурных частиц (атомов, молекул). Единицей количества вещества является – моль. 1 моль = количеству вещества, содержащего столько же структурных частиц, сколько атомов содержится в углероде.
Na = 6,02 * 1023 [ 1/моль; моль -1]
Объёмная доля компонента в веществе – безразмерная физическая величина, равная отношению приведённого объёма компонента к общему объёму вещества.
Молярная концентрация – отношение количества растворённого вещества к объёму раствора.
[моль/дм3]
Относительная плотность одного газа по другому – безразмерная величина, показывающая во сколько раз один газ тяжелее или легче другого.
Закон Авогадро – основной газовый закон (был высказан как гипотеза в 1811 г. итальянским физиком, химиком А. Авогадро и интерпретирован с точки зрения атомно-молекулярного учения в 1858 г. итальянским химиком С. Канниццаро)
Первое следствие из закона Авогадро: В частности, при нормальных условиях (н. у.) - температуре Т = 273,15 K (0 °С) и давлении р = 1,01325 · 105 Па (1 атм, 760 мм. рт. ст.) - 1 моль любого газа (близкого по свойствам к идеальному газу), занимает объём 22,4 л. Эта физическая постоянная – молярный объём газа при нормальных условиях. Второе следствие из закона Авогадро: MB = Mвозд · Dвозд = 29Dвозд |
Поиск
Архив записей
|
|