Статистика

Онлайн всего: 1 Гостей: 1 Пользователей: 0
|
Типы расчетных задач по химии по годам обучения: 10 класс
1.
Расчеты
содержания элементов в веществе по его формулам (в граммах, молях и массовых
долях).
Пример 11.
Из образца горной породы массой 25
г, содержащего минерал аргентит Ag2S, выделено серебро массой 5,4 г. Определите массовую
долю аргентита в образце.
|
Дано:
m(образца) = 25 г
m(Ag) = 5,4 г
|
Решение
1. Для решения используем формулы: n =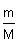 ; m = n· M; ; m = n· M;
w(X) =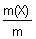 . .
2. Находим химическое количество выделенного серебра:
n(Ag) =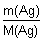 = = 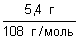 = 0,05 моль = 0,05 моль
3. Находим химическое количество аргентита:
n(Ag2S)
: n(Ag) = 1 : 2
n(Ag2S) = 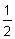 n(Ag) = n(Ag) = 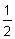 · 0,05 моль = 0,025 моль. · 0,05 моль = 0,025 моль.
4. Определяем массу аргентита в образце горной породы:
Mr(Ag2S)
= 2Ar(Ag)+Ar(S) = 2·108 + 32 =248; M(Ag2S)=
248 г/моль
m(Ag2S) = n(Ag2S)
· M(Ag2S) = 0,025 моль · 248 г/моль = 6,2 г.
5. Находим массовую долю аргентита в образце горной породы:
w(Ag2S) = 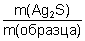 = = 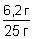 = 0,248 (24,8%); = 0,248 (24,8%);
Ответ: массовая доля аргентита в
образце горной породы составляет 24,8%.
|
|
Найти
w(Ag2S)
|
2.
Установление
эмпирической и молекулярной (истинной) формул по массовым долям элементов,
входящих в состав вещества.
Пример 12.
Установите молекулярную формулу вещества, если массовая доля углерода в нем
составляет 26,67%, водорода – 2,22%, кислорода – 71,11%. Относительная
молекулярная масса этого вещества равна 90.
|
Дано:
CxHyOz
w(C) = 0,2667 (26,67%)
w(H) = 0,0222 (2,22%)
w(O) = 0,7111 (71,11%)
Mr(CxHyOz)
= 90
|
Решение
1. Для решения задачи используем формулы: w =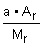 ; ;
n
=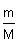 ; x :
y : z = n(C) : n(H) : n(O). ; x :
y : z = n(C) : n(H) : n(O).
2. Находим химические количества элементов, входящих в состав
вещества, приняв, что m(CxHyOz) = 100 г.
m(C) = w(C) · m(CxHyOz) = 0,2667 · 100 г = 26,67 г.
m(H) = w(H) · m(CxHyOz) = 0,0222 · 100 г = 2,22 г.
m(O) = w(O) · m(CxHyOz) = 0,7111 · 100 г = 71,11 г.
n(C) = 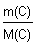 = = 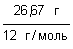 = 2,22 моль. = 2,22 моль.
n(H) = 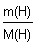 = = 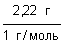 = 2,22 моль. = 2,22 моль.
n(O) = 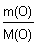 = = 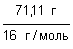 = 4,44 моль. = 4,44 моль.
3. Определяем эмпирическую формулу вещества:
n(C) : n(H) : n(O) = 2,22 моль : 2,22 моль : 4,44
моль.
x : y : z = 1 : 1 : 2.
Эмпирическая
формула вещества – CHO2.
4. Устанавливаем истинную молекулярную формулу вещества:
Mr(CHO2)
= Ar(C) + Ar(H) + 2Ar(O) = 12 + 1 + 2·16 =
45;
Mr(CHO2) : Mr(CxHyOz) = 45 : 90 = 1 : 2.
Истинная
молекулярная формула вещества – C2H2O4.
Ответ: молекулярная формула вещества C2H2O4.
|
|
Найти
x, y, z
|
3.
Вычисление
по уравнению химической реакции объемов газов по известному химическому
количеству одного из веществ.
Пример 13. Какой
объем водорода (н.у.) выделится при реакции цинка химическим количеством 0,5
моля с избытком раствора соляной кислоты?
|
Дано:
n(Zn) = 0,5 моль
|
Решение
1. Составляем уравнение реакции цинка с раствором
соляной кислоты:
0,5 моля 0,5
моля
Zn
+ 2HCl = ZnCl2
+ H2
1 моль 1 моль
2. Для решения
используем формулу: V = n · Vm.
3. По уравнению реакции находим химическое количество выделившегося
водорода: n(H2) = n(Zn) = 0,5 моль.
4. Определяем объем выделившегося водорода:
V(H2) = n(H2) · Vm = 0,5 моль · 22,4 дм3/моль
= 11,2 дм3.
Ответ: выделится водород объемом 11,2
дм3.
|
|
Найти
V(H2)
|
4.
Расчет
объемных отношений газообразных веществ по химическим уравнениям.
Пример 14. Какой
объем оксида углерода(IV) образуется при сгорании ацетилена объемом 5 дм3(н.у.)?
|
Дано:
V(C2H2)
= 5 дм3
|
Решение
1. Составляем уравнение реакции горения ацетилена:
5
дм3 X дм3
2C2H2 + 5O2
= 4CO2 + 2H2O
2V 4V
2. Для решения, согласно закону объемных отношений газов
при химических реакциях,
используем формулу: V(C2H2) : V(CO2) = 2 : 4;
V(C2H2) : V(CO2) = 1 : 2.
3. Определяем объем выделившегося водорода:
V(CO2) = 2V(C2H2) = 2· 5 дм3 = 10 дм3.
Ответ: образуется оксид углерода(IV) объемом 10 дм3.
|
|
Найти
V(CO2)
|
|
Календарь
| « Май 2024 » | | Пн | Вт | Ср | Чт | Пт | Сб | Вс | | | | 1 | 2 | 3 | 4 | 5 | | 6 | 7 | 8 | 9 | 10 | 11 | 12 | | 13 | 14 | 15 | 16 | 17 | 18 | 19 | | 20 | 21 | 22 | 23 | 24 | 25 | 26 | | 27 | 28 | 29 | 30 | 31 |
|