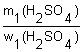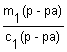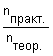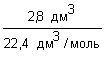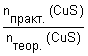1. Расчет массы (объема вещества), необходимого для приготовления раствора с заданной массовой долей (молярной концентраций).
Пример 19. Какой
объем раствора серной кислоты плотностью 1,8 г/см3 с массовой долей H2SO4 88% нужно взять для приготовления
раствора кислоты объемом 300 см3 и плотностью 1,3 г/см3 с
массовой долей H2SO4 40%?![]()
|
Дано: w1(H2SO4) = 0,88 (88%) ρ1(р-ра) = 1,8 г/см3 w2(H2SO4) = 0,4 (40%) ρ2(р-ра) = 1,3 г/см3 V2(р-ра) = 300 см3 |
Решение 1. Для решения задачи используем формулы: w(в-ва) = 2. Определяем массу полученного раствора и массу H2SO4 в нем: m2(р-ра) = ρ2(р-ра) · V2(р-ра) = 1,3 г/см3 · 300 см3 = 390 г. m2(H2SO4) = m2(р-ра) · w2(H2SO4) = 390 г · 0,4 = 156 г. 3. Находим массу и объем исходного раствора: m1(H2SO4) = m2(H2SO4) = 156 г. m1(р-ра) = V1(р-ра) = Ответ: потребуется раствор кислоты объемом 98,5 см3. |
|
Найти V1(р-ра) |
Пример 20. Какой объем раствора серной кислоты плотностью 1,035 г/см3 с массовой долей H2SO4 5,5% нужно взять для приготовления раствора серной кислоты объемом 300 см3 с молярной концентрацией H2SO4 0,25 моль/дм3?
|
Дано: w1(H2SO4) = 5,5 (0,055%) ρ1(р-ра) = 1,035 г/см3 с2(H2SO4) = 0,25 моль/дм3 V2(р-ра) = 300 см3 |
Решение 1. Для решения задачи используем формулы: c(X) = 2. Находим химическое количество H2SO4 в полученном растворе: n2(H2SO4) = c2(H2SO4) · V2(р-ра) = 0,25 моль/дм3 · 0,3 дм3 = = 0,075 моль. 3. Находим массу H2SO4 в исходном растворе: n1(H2SO4) = n2(H2SO4) = 0,075 моль. Mr(H2SO4) = 2Ar(H) + Ar(S) + 4Ar(O) = 2·1 + 32 + 4·16 = 98 M(H2SO4) = 98 г/моль. m2(H2SO4)= n2(H2SO4)· M(H2SO4)= 0,075 моль · 98 г/моль = = 7,35 г. 4. Находим массу и объем исходного раствора: m1(р-ра) = V1(р-ра) = Ответ: потребуется раствор кислоты объемом 129,1 см3. |
|
Найти V1(р-ра) |
2. Определение практического выхода продукта реакции.
Пример 21. При пропускании сероводорода объемом 2,8 дм3 (при н.у.) через избыток раствора сульфата меди(II) образовался осадок массой 11,4 г. Вычислите выход продукта реакции.
|
Дано: V(H2S) = 2,8 дм3 m практ.(CuS) = 11,4 г |
Решение 1. Составляем уравнение реакции нейтрализации:
0,125 моль 0,125 моль
CuSO4 + H2S = CuS↓ + H2SO4
1 моль 1 моль
2. Для решения задачи используем формулы: η = 3. Находим химическое количество сероводорода: n(H2S) = 4. Определяем химические количества сульфида меди(II) (теоретически возможное и практически полученное): nтеор.(CuS) = n(H2S) = 0,125 моль. Mr(CuS) = Ar(Cu) + Ar(S) = 64 + 32 = 96 M(CuS) = 96 г/моль. nпракт.(CuS) = 5. Вычислите выход продукта реакции. η(CuS) = Ответ: выход продукта реакции составляет 95,2%. |
|
Найти V1(р-ра) |