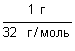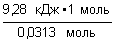1. Вычисление относительной плотности и молярной массы газов.
Пример 15. Вычислите молярную массу газа, относительная плотность которого по водороду равна 32. Рассчитайте относительную плотность этого газа по воздуху.
|
Дано:
M(возд.) » 29 г/моль |
Решение 1. Для решения используем формулу: 2. Вычисляем молярную массу газа: M(газа) = 3. Определяем относительную плотность газа по воздуху: Ответ: молярная масса газа – 64 г/моль, относительная плотность этого газа по воздуху – 2,207. |
|
Найти M(газа)
|
2. Вычисление молярной концентрации газов.
Пример 16. В сосуд объемом 5 дм3 поместили газообразные вещества: A (химическим количеством 2 моль) и B (химическим количеством 3 моль). Вычислите молярные концентрации этих веществ в смеси.
|
Дано: V = 5 дм3 n(A) = 2 моль n(B) = 3 моль |
Решение 1. Для решения используем формулу: c(X) = 2. Вычисляем молярные концентрации газов: c(A) = c(B) = Ответ: молярная концентрация вещества A – 0,4 моль/дм3, а молярная концентрация вещества B – 0,6 моль/дм3. |
|
Найти c(A), c(B) |
3. Расчеты по термохимическим уравнениям.
Пример 17. При сжигании серы массой 1 г выделилось количество теплоты 9,28 кДж. Составьте термохимическое уравнение реакции.
|
Дано: m(S) = 1 г Q' = 9,28 кДж |
Решение 1. Составляем уравнение термохимическое реакции горения серы:
0,0313 моль +9,28 кДж S + O2 = SO2 ± Q 1 моль 2. Для решения задачи используем формулу: n = 3. Находим химическое количество серы: n(S) = 3. Находим тепловой эффект реакции горения серы и составляем термохимическое уравнение: Q
= S + O2 = SO2 + 296,5 кДж Ответ: S + O2 = SO2 + 296,5 кДж |
|
Найти Q |
4. Вычисления по уравнениям реакций, протекающих в растворах.
Пример 18. Какая масса раствора соляной кислоты с массовой долей HCl 20% потребуется для нейтрализации раствора гидроксида натрия массой 45 г с массовой долей NaOH 15%?
|
Дано: w(HCl) = 0,2 (20%) w(NaOH) = 0,15 (15%) mр-ра(NaOH) = 45 г |
Решение 1. Составляем уравнение реакции нейтрализации:
0,169 моль 0,169 моль
NaOH + HCl = NaCl + H2O
1 моль 1 моль 2. Для решения
используем формулы: w(в-ва) = n = 3. Вычисляем массу и химическое количество NaOH: m(NaOH) = mр-ра(NaOH) · w(NaOH) = 45 г · 0,15 = 6,75 г Mr(NaOH) = Ar(Na) + Ar(O) + Ar(H) = 23 + 16 + 1 = 40; M(NaOH) = 40 г/моль; n(NaOH) = 4. Определяем по уравнению реакции химическое количество HCl: n(HCl) = n(NaOH) = 0,169 моль. 5. Вычисляем массу чистого вещества и массу раствора HCl: Mr(HCl) = Ar(H) + Ar(Cl) = 1 + 35,5 = 36,5; M(HCl) = 36,5 г/моль; m(HCl) = n(HCl) · M(HCl) = 0,169 моль · 36,5 г/моль = 6,2 г mр-ра(HCl) = Ответ: потребуется раствор соляной кислоты массой 31 г. |
|
Найти mр-ра(HCl) |