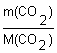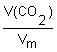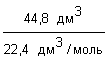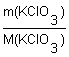7 класс
1. Вычисление относительной молекулярной и относительной формульной масс веществ по химическим формулам [4].
Пример 1. Вычислите относительные молекулярные массы веществ: H2S, HNO3, C6H12O6 и относительные формульные массы веществ: Fe2O3, K2CO3, Cu(NO3)2.
Решение. Mr(H2S) = 2Ar(H) + Ar(S) = 2·1 + 32 = 34;
Mr(HNO3) = Ar(H) + Ar(N) + 3Ar(O) = 1+ 14 + 3·16 = 63;
Mr(C6H12O6) = 6Ar(C) + 12Ar(H) + 6Ar(O) = 6·12 + 1·12 + 6·16 = 180;
Mr(Fe2O3) = 2Ar(Fe) + 3Ar(O) = 2·56 + 3·16 = 160;
Mr(K2CO3) = 2Ar(K) + Ar(C) + 3Ar(O) = 2·39 + 12 + 3·16 = 138;
Mr(Cu(NO3)2) = Ar(Cu) + 2(Ar(N) + 3Ar(O)) = 64 + 2(14 + 3·16) = 188.
2. Вычисление массовой доли элемента по формуле вещества.
Пример 2. Вычислите массовые доли элементов в серной кислоте.
|
Дано: H2SO4 |
Решение 1. Для решения задачи используем формулу: w = 2. Вычисляем относительную молекулярную массу серной кислоты: Mr(H2SO4) = 2Ar(H) + Ar(S) + 4Ar(O) = 2·1 + 32 + 4·16 = 98; 3. Определяем массовые доли каждого элемента: w(H)
= w(S) = w(O) = 100% - w(H) - w(S) = 100% - 2% - 33% = 65%. Ответ: w(H) = 2%; w(S) = 2%; w(O) = 65%. |
|
Найти w(H), w(S), w(O) |
3. Вычисление химического количества вещества по его массе и массы вещества по его химическому количеству.
Пример 3. Вычислите химическое количество углекислого газа массой 8,8 г.
|
Дано: m(CO2) = 8,8 г |
Решение 1. Для решения задачи используем формулу: n = 2. Вычисляем молярную массу CO2: Mr(CO2) = Ar(C) + 2Ar(O) = 12+ 2·16 = 44; M(CO2) = 44 г/моль; 3. Определяем химическое количество CO2: n(CO2) = Ответ: химическое количество углекислого газа массой 8,8 г составляет 0,2 моль. |
|
Найти n(CO2) |
Пример 4. Вычислите массу углекислого газа, химическое количество которого составляет 0,2 моль.
|
Дано: n(CO2) = 0,2 моль |
Решение 1. Для решения задачи используем формулу: m = n· M. 2. Вычисляем молярную массу CO2: Mr(CO2) = Ar(C) + 2Ar(O) = 12+ 2·16 = 44; M(CO2) = 44 г/моль; 3. Определяем массу CO2: m(CO2) = n(CO2) · M(CO2) = 0,2 моль· 44 г/моль = 8,8 г; Ответ: масса порции углекислого газа химическим количеством 0,2 моль равна 8,8 г. |
|
Найти m(CO2) |
4. Вычисление химического количества газа по его объему и объема газа по его химическому количеству.
Пример 5. Вычислите химическое количество углекислого газа объемом 4,48 дм3.
|
Дано: V(CO2) = 4,48 дм3 |
Решение 1. Для решения задачи используем формулу: n = 2. Определяем химическое количество CO2: n(CO2) = Ответ: химическое количество углекислого газа объемом 8,8 дм3 составляет 0,2 моль. |
|
Найти n(CO2) |
Пример 6.
Вычислите объем углекислого газа, химическое количество которого составляет 0,2
моль.![]()
|
Дано: n(CO2) = 0,2 моль |
Решение 1. Для решения задачи используем формулу: V = n· Vm. 2. Определяем объем CO2: V(CO2) = n(CO2) · Vm = 0,2 моль· 22,4 дм3/моль = 44,8 дм3; Ответ: объем порции углекислого газа химическим количеством 0,2 моль равен 44,8 дм3. |
|
Найти V(CO2) |
5. Вычисление по химическим уравнениям массы, химического количества и объема (для газов) по известным массе, химическому количеству и объему (для газов) одного из вступивших в реакцию или полученных веществ.
Пример 7. Вычислите массу хлорида калия и объем кислорода, образовавшихся в результате реакции разложения хлората калия (KClO3) массой 4,9 г.
|
Дано: m(KClO3) = 4,9 г |
Решение 1. Составляем уравнение реакции разложения хлората калия:
0,04 моль 0,04 моль 0,06 моль 2KClO3
2 моль 2 моль 3 моль 2. Для решения
используем формулы: n = |
|
Найти m(KCl), V(O2) |
|
|
|
3. Вычисляем молярные массы KClO3 и KCl: Mr(KClO3) = Ar(K) + Ar(Cl) + 3Ar(O) = 39 + 35,5 + 3·16 = 122,5; M(KClO3) = 122,5 г/моль; Mr(KCl) = Ar(K) + Ar(Cl) = 39 + 35,5 = 74,5; M(KCl) = 74,5 г/моль; 4. Определяем химическое количество KClO3: n(KClO3) = 5. По уравнению реакции находим химические количества образовавшихся KCl и O2: n(KCl) = n(KClO3) = 0,04 моль; n(O2)= 1,5n(KClO3) = 0,06 моль; 6. Вычисляем массу хлорида калия и объем кислорода: m(KCl) = n(KCl) · M(KCl) = 0,04 моль · 74,5 г/моль = 2,98 г; V(O2) = n(O2) · Vm = 0,06 моль· 22,4 дм3/моль = 1,34 дм3. Ответ: образуется хлорид калия массой 2,98 г составляет кислород объемом 1,34 дм3. |